| Главная » Статьи » Некоронарогенные заболевания сердца » Инфильтративные заболевания миокарда |
Редкий случай транстиретинового амилоидоза с поражением сердца и распространенными системными проявлениями Авторы: С.А.Болдуева, М.В.Самохвалова, А.Д.Хомуло, В.В.Зайцев, В.А.Маринин, С.А.Винничук Журнал: CardioСоматика. 2017; 8 (4): 42–46.
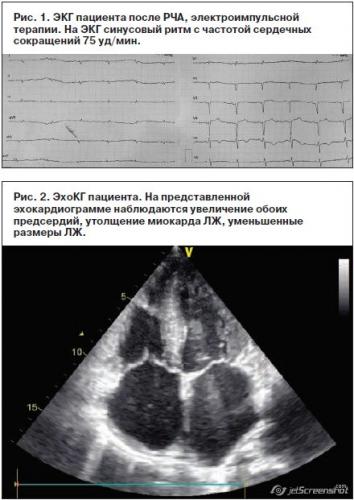
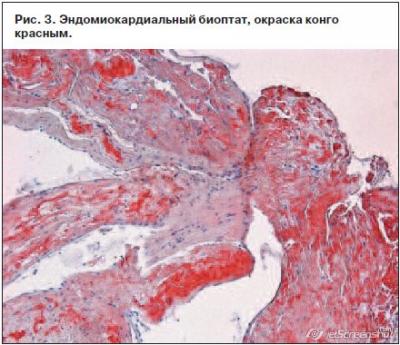
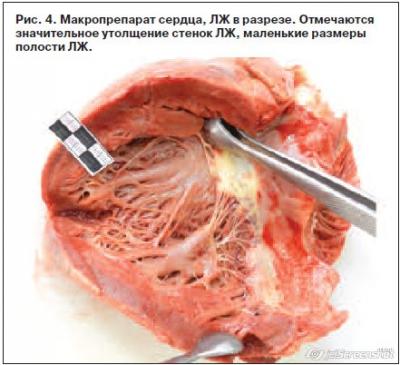
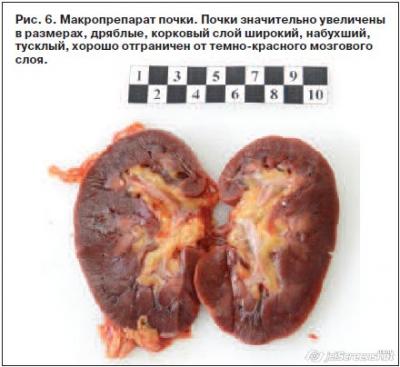
Амилоидоз – это заболевание, при котором в органах и тканях происходит отложение амилоида – особого патологического белка фибриллярной структуры. В зависимости от вида белка, формирующего амилоид, выделяют несколько форм заболевания [1]. Сердце наиболее часто поражается при первичном AL-амилоидозе, в этом случае амилоид представлен легкими цепями иммуноглобулинов [2]. Вовлечение сердца в патологический процесс встречается также при транстиретиновом амилоидозе (ТТА), имеющем такие формы, как сенильный кардиальный амилоидоз, системный семейный амилоидоз и др. [3]. При ТТА субстратом для образования амилоида является белок транстиретин, который присутствует в человеческом организме в нормальных условиях и отвечает за транспорт транстиретина в ткани из печени, где он преимущественно образуется. При определенных условиях транстиретин способен к агрегации и образованию нитей амилоида, которые откладываются в органах и тканях, оказывая повреждающее и токсическое действие. Помимо сердца для ТТА характерна прогрессирующая периферическая нейропатия, реже – поражение других органов. Существуют 2 основные формы ТТА: мутантная форма и «дикий» тип. В настоящее время описано более 60 мутаций транстиретина, которые определяют клиническую картину заболевания [3]. Амилоидная инфильтрация сердца при ТТА приводит к утолщению стенок миокарда, нарушению его расслабления и развитию рестриктивной кардиомиопатии. Клинические проявления характеризуются бивентрикулярной хронической сердечной недостаточностью (ХСН), нарушениями ритма и проводимости [4]. Амилоидная периферическая нейропатия при ТТА является симметричной, восходящей (аксональный тип) и нередко сочетается с автономной нейропатией, которая протекает с явлениями ортостатической гипотензии и синкопальными состояниями [3]. Прогноз ТТА определяется вовлечением сердца, однако если при AL-амилоидозе медиана выживаемости от начала клинических проявлений ХСН составляет 5–6 мес [5], то при ТТА – 60–75 мес [6, 7]. Важно отметить, что у половины больных с ТТА наблюдается карпальный туннельный синдром, связанный с отложением амилоида в синовиальных оболочках суставов и сухожилиях кистей, причем эти проявления предшествуют развитию амилоидной кардиомиопатии за 8–10 лет [8]. Диагноз ТТА подтверждается с помощью гистологического (окраска биоптата конго красным, тио-флавином) и иммуногистохимического методов. Из неинвазивных методов используются эхокардиография, магнитно-резонансная томография, сцинтиграфия миокарда [3]. В последние годы в лечении ТТА появились обнадеживающие результаты, связанные с применением новых фармакологических средств [9–12], а также – трансплантации печени и сердца [13–17]. Ранняя диагностика заболевания и своевременно начатое лечение могут стабилизировать патологический процесс. Описание клинического случая Приводим наблюдавшийся в нашей практике случай ТТА с множественными системными поражениями, включая сердце. Пациент 46 лет поступил в клинику с жалобами на одышку при небольших физических нагрузках (ходьба на расстояние 20–50 м), приступы удушья в покое в горизонтальном положении тела, выраженную общую слабость, быструю утомляемость, периодически появляющиеся геморрагические высыпания вокруг глаз и на теле, особенно в области шеи, неинтенсивный кожный зуд. При опросе по системам и органам удалось выяснить, что по утрам беспокоит кашель с периодическим отхождением вязкой желто-зеленой мокроты в небольшом количестве; отмечает сухость и периодически появляющуюся горечь во рту, изжогу, вздутие живота, склонность к запорам. Из анамнеза известно, что в течение года отмечалось появление немотивированной слабости, похудел на 10 кг. Полгода назад стал отмечать периодическое появление геморрагических высыпаний на коже лица, шеи, подмышечных впадинах, по поводу чего к врачам не обращался. За 2 мес до настоящей госпитализации появились одышка при физических нагрузках, отеки голеней и стоп. В связи с внезапно развившимся ночью приступом удушья был госпитализирован в больницу по месту жительства, где было выявлено трепетание предсердий (ТП). При обследовании данных за ишемическую болезнь сердца и гипертоническую болезнь не получено. Была выполнена эхокардиография (ЭхоКГ): аорта на уровне синусов 34 мм, в восходящем отделе 33 мм, межжелудочковая перегородка 16 мм, задняя стенка левого желудочка (ЛЖ) 13 мм, конечно-диастолический объем ЛЖ 36 мл, конечно-систолический объем ЛЖ 18 мл, ударный объем 18 мл, фракция выброса (Симпсон) 50%, объем левого предсердия (ЛП) 68 мл, объем правого предсердия (ПП) 63 мл, митральная недостаточность 2-й степени, трикуспидальная недостаточность 3-й степени. Состояние было расценено как бивентрикулярная ХСН на фоне тахисистолической формы ТП, рекомендовано выполнение радиочастотной абляции (РЧА). После выписки у пациента сохранялись жалобы на одышку при умеренных физических нагрузках, отеки обеих голеней. Для выполнения РЧА пациент был госпитализирован в аритмологическое отделение ФГБОУ ВО «СЗГМУ им. И.И.Мечникова». Из анамнеза жизни известно, что курил в течение многих лет, употреблял алкоголь в избыточном количестве, не женат, о заболеваниях ближайших родственников ничего не знает. При поступлении в клинику по объективным данным состояние пациента расценено как средней степени тяжести. Пациент астенического телосложения, имеет место дефицит массы тела. Кожные покровы с диффузной гиперпигментацией, нормальной влажности, акроцианоз, наблюдаются геморрагические высыпания в области шеи и плечевого пояса, определяются набухшие шейные вены. Пульс 100 ударов в 1 мин, аритмичный, удовлетворительного наполнения и напряжения. Артериальное давление на обеих руках 90/60 мм рт. ст. Тоны сердца приглушены, систолический шум над мечевидным отростком. В легких – дыхание жесткое, хрипы не выслушиваются. Язык увеличен в объеме, с отпечатками зубов, имеется грязно-желтый налет. Живот увеличен в объеме за счет асцита, при пальпации мягкий, безболезненный. Печень на 3 см выступает из-под края реберной дуги, плотная, край острый. Пальпируется нижний полюс селезенки, край плотный, безболезненный. Поколачивание по поясничной области безболезненное, почки не пальпируются. На электрокардиограмме (ЭКГ), снятой в момент госпитализации: ТП с частотой желудочковых ответов 78 в 1 мин, сниженный вольтаж комплексов QRS во всех отведениях. В анализах крови – гемоглобин (115 г/л), лейкоцитоз (14,6×109/л), тромбоциты (264×109/л); гипопротеинемия (54 г/л), повышение печеночных ферментов (аланинаминотрансфераза 211 Е/л, аспартатаминотрансфераза 149 Е/л), билирубина (20 мкмоль/л), щелочной фосфатазы (312 Е/л), g-глутамилтранспептидазы (227 Е/л), протромбинового индекса (44%), креатинина (120 мкмоль/л), мочевины (13 ммоль/л); скорость клубочковой фильтрации (60 мл/мин). В общем анализе мочи: лейкоцитурия (20/мкл), гематурия (56/мкл), протеинурия (1,34 г/л). Суточная потеря белка 3,5 г/сут. На следующий день после госпитализации выполнена РЧА кавотрикуспидального истмуса, ритм восстановить не удалось. Синусовый ритм восстановлен с помощью электроимпульсной терапии (рис. 1). На 2-е сутки после оперативного лечения пациент отметил резкое ухудшение самочувствия, выражающееся в нарастании одышки, отеков на фоне выраженной гипотензии, в связи с чем был переведен в отделение реанимации и интенсивной терапии. На рентгенограмме грудной полости, сидя справа, нечеткий контур диафрагмы, затемнен синус – возможно наличие жидкости в плевральной полости, слева в нижних отделах понижена воздушность, но отчетливо инфильтративных изменений не выявлено, синус свободен. В остальных отделах легочные поля воздушны. Тень сердца не смещена, сглажена левая дуга за счет выбухания легочной артерии, расширены левые отделы. По данным ультразвукового исследования органов брюшной полости и почек – эхографические признаки диффузных изменений печени (структура неоднородная, мелкозернистая, эхогенность повышена умеренно, размеры 150×60 см), поджелудочной железы (структура неоднородная, мелкозернистая, эхогенность чуть выше печени), утолщение стенки и деформация желчного пузыря, значительное количество жидкости в брюшной полости вокруг печени, селезенки, в боковых каналах, малом тазе; эхографические признаки диффузных изменений почек. Размеры селезенки 106×45 см. При фиброгастродуоденоскопии выявлены недостаточность кардии, язвенная болезнь желудка – язва задней стенки желудка; рубцово-язвенный стеноз пилоробульбарного отдела; эрозивно-геморрагический гастродуоденит, обострение. По данным ЭхоКГ (рис. 2): ЛЖ уменьшен в размерах (конечно-диастолический размер 37 мм, конечно-систолический размер 28 мм, конечно-диастолический объем 50 мл, конечно-систолический объем 25 мл), концентрическая гипертрофия ЛЖ (межжелудочковая перегородка 15 мм, задняя стенка ЛЖ 16 мм), диффузная гипокинезия миокарда, фракция выброса 50%, увеличение ЛП (46 мм, индекс ЛП 27), митральная регургитация 1–2-й степени, ПП расширено (51×64 мм), стенки ПЖ утолщены (размер 25 мм), трикуспидальная недостаточность 3-й степени, давление в легочной артерии не повышено, рестриктивный тип диастоличсекой дисфункции, расхождение листков перикарда за ПП 5 мм. На фоне диуретической терапии и инотропной поддержки отмечались некоторая положительная динамика, уменьшение отеков и одышки. Для дальнейшего обследования и лечения пациент был переведен в кардиологическое отделение. Учитывая системность клинических проявлений – тяжелая бивентрикулярная ХСН, ТП, устойчивое к РЧА, признаки поражения печени (печеночно-клеточная недостаточность с признаками цитолиза) и почек (нефротический синдром, гематурия), кожи (сыпь геморрагического характера), макроглоссия, а также данные ЭКГ (существенное снижение вольтажа, рубцово-подобные изменения) и главным образом – результаты ЭхоКГ (утолщение стенок ЛЖ и ПЖ с уменьшением полости ЛЖ, увеличение размеров предсердий, рестриктивный тип наполнения желудочков) – был заподозрен первичный системный амилоидоз с поражением сердца. В связи с этим больному была выполнена биопсия миокарда, результаты которой оценивались в НИИ патоморфологии ФГБУ «НМИЦ им. В.А.Алмазова» профессором Л.Б.Митрофановой. Использовались окраски гематоксилин-эозином, конго красным, ШИК-реакция, окраска по Ван Гизону. Результаты гистологического исследования (рис. 3): неравномерная гипертрофия мышечных волокон, умеренная дистрофия-дегенерация кардиомиоцитов без явных некрозов, отложения белковых депозитов под эндокардом, периваскулярно, перимускулярно во всех биоптатах. Белок имеет кирпично-красное окрашивание при окраске конго красным и яблочно-зеленое свечение при поляризационной микроскопии. По данным гистохимического исследования λk-легких целей не выявлено, установлен диагноз транстеритинового амилоидоза. Генотипирование не выполнялось. На фоне проводимой терапии у больного сохранялись отечный синдром в виде периферических отеков, гидроторакса и асцита, явления почечной и печеночной недостаточности, нарастала потеря массы тела. В связи с выраженной ортостатической гипотензией и пресинкопальными состояниями консультирован неврологом, установлен диагноз периферической полинейропатии, автономной нейропатии вследствие основного заболевания. Проводились массивная мочегонная терапия на фоне инотропной поддержки, инфузии альбумина, парентеральное питание; были добавлены глюкокортикоиды, на фоне которых наблюдалось кратковременное улучшение: стабилизация артериального давления на уровне 90–100/70 мм рт. ст., увеличение диуреза, уменьшение отечного синдрома и одышки. Обсуждался вопрос об ультрафильтрации, однако, учитывая нефротический синдром, от проведения ультрафильтрации отказались. В связи с тяжестью состояния больного вопрос о химиотерапии и трансплантации органов не стоял. В последующем рецидивировали пароксизмы ТП, на фоне которых наросли явления ХСН, почечной и печеночной недостаточности и через 7 нед после поступления на фоне полиорганной недостаточности развилась асистолия и констатирована биологическая смерть. Клинический диагноз. Основной: системный (транстиретиновый) амилоидоз с поражением сердца, почек, печени, селезенки, языка, надпочечников (последнее предполагалось в связи с гиперпигментацией кожи и выраженной гипотензией), периферической и автономной нервной системы. Осложнение: ХСН IV функционального класса, III стадии. Персистирующая форма ТП, РЧА, повторная электроимпульсная терапия. Сопутствующий: язвенная болезнь желудка, обострение. Язва желудка. Эрозивный гастродуоденит. Рубцово-язвенный стеноз пилоробульбарного отдела. Хроническая обструктивная болезнь легких. Хронический бронхит, вне обострения, ремиссия. Хронический панкреатит, вне обострения. По результатам патологоанатомического исследования выявлялись массивные отложения амилоида в сердце (рис. 4), печени (рис. 5), почках (рис. 6), селезенке, языке, тонком и толстом кишечнике и был установлен следующий диагноз: • Основной – ТТА (гистологическое исследование) с поражением сердца, почек, печени, селезенки, языка, тонкой и толстой кишки. • Осложнение – истощение: толщина подкожной жировой клетчатки на передней брюшной стенке 1 см, атрофия скелетных мышц. Отеки мягких тканей нижних конечностей. Гидроторакс: справа и слева по 100 мл. Асцит 2500 мл. Резко выраженная паренхиматозная дистрофия внутренних органов. Отек легких. Отек головного мозга. • Сопутствующий – язвенная болезнь двенадцатиперстной кишки – хроническая рубцующаяся язва луковицы двенадцатиперстной кишки. Хронический панкреатит: солитарные кисты (1,5 и 2 см в диаметре), фиброз и атрофия ткани поджелудочной железы. Атеросклероз аорты, коронарных, церебральных, почечных артерий. Заключение Таким образом, у больного наблюдались выраженные системные проявления амилоидоза с поражением сердца, и на момент поступления в кардиологическое отделение ФГБОУ ВО «СЗГМУ им. И.И.Мечникова» диагноз не вызывал больших трудностей. На наш взгляд, и во время первой госпитализации по поводу ТП докторам следовало обратить внимание на данные ЭхоКГ, при которой у пациента при отсутствии в анамнезе гипертонической болезни выявлялись признаки значительного утолщения стенок ЛЖ (а как оказалось при обследовании через 2 нед – и утолщение стенок ПЖ), уменьшение полости ЛЖ, увеличение обоих предсердий, рестриктивный тип наполнения желудочков и при этом на ЭКГ не было признаков гипертрофии ЛЖ, но отмечался низкий вольтаж зубцов. Судя по имеющимся системным проявлениям, которые выявлялись через 2 нед после первой госпитализации, последние, очевидно, имели место и ранее, но были объяснены ХСН. Хотя такие жалобы, как геморрагическая сыпь, макроглоссия, спленомегалия, нефротический синдром, требовали другой интерпретации. Наджелудочковые нарушения ритма нередко встречаются при амилоидном поражении сердца, что объясняется изменением размеров и структуры предсердий, и усугубляют течение ХСН, которая развивается вследствие вторичной рестриктивной кардиомиопатии. Явления периферической нейропатии, характерные для ТТА, у данного больного были выражены умеренно, а вот системная и ортостатическая гипотензия, развивающиеся вследствие автономной нейропатии, были представлены. Выраженная гипотензия препятствовала использованию всего спектра медикаментозной терапии ХСН и ухудшила прогноз болезни. Вместе с тем ранняя диагностика системного амилоидоза дает пациентам шанс получить современные методы лечения заболевания и продлить жизнь. Для цитирования: С.А.Болдуева, М.В.Самохвалова, А.Д.Хомуло, В.В.Зайцев, В.А.Маринин, С.А.Винничук. Редкий случай транстиретинового амилоидоза с поражением сердца и распространенными системными проявлениями. Кардиосоматика. 2017; 04: 42-46 Сведения об авторах: Болдуева Светлана Афанасьевна – д-р мед. наук, проф., зав. каф. факультетской терапии ФГБОУ ВО «СЗГМУ им. И.И.Мечникова». E-mail: svetlanaboldueva@mail.ru Самохвалова Марина Витальевна – канд. мед. наук, зав. кардиологическим отд-нием клиник ФГБОУ ВО «СЗГМУ им. И.И.Мечникова» Хомуло Арина Дмитриевна – врач-кардиолог кардиологического отд-ния клиник ФГБОУ ВО «СЗГМУ им. И.И.Мечникова» Зайцев Вадим Витальевич – врач-кардиолог главного клинического комплекса ФГБУ «НМИЦ им. В.А.Алмазова» Маринин Валерий Алексеевич – зав. аритмологическим отд-нием клиник ФГБОУ ВО «СЗГМУ им. И.И.Мечникова» Винничук Сергей Анатольевич – зав. патологоанатомическим отд-нием клиники, канд. мед. наук, доц. каф. патологической анатомии ФГБОУ ВО «СЗГМУ им. И.И.Мечникова» Список использованной литературы: 1. Шилов Е.М. Нефрология. 2-е изд., испр. и доп. М.: ГЭОТАР-Медиа, 2010; с. 352–70. / Shilov E.M. Nefrologiia. 2-e izd., ispr. I dop. M.: GEOTAR-Media, 2010; s. 352–70. [in Russian] 2. Лутай М.И. и др. Амилоидоз сердца: трудный диагноз. Здоровая Украина. 2012; с. 34–7. / Lutai M.I. i dr. Amiloidoz serdtsa: trudnyi diagnoz. Zdorovaia Ukraina. 2012; s. 34–7. [in Russian] 3. Diagnosis, Prognosis, and Therapy of Transthyretin Amyloidosis. J Am Coll Cardiol 2015; 66 (21): 2451–66. 4. Болдуева С.А., Самохвалова М.В., Богданова Е.В., Соловьева Т.C. Первичный системный амилоидоз с поражением сердца и коронарных артерий. Кардиология. 2010; 6: 92–4. / Boldueva S.A., Samokhvalova M.V., Bogdanova E.V., Solov'eva T.C. Pervichnyi sistemnyi amiloidoz s porazheniemserdtsa i koronarnykh arterii. Kardiologiia. 2010; 6: 92–4. [in Russian] 5. Connors LH, Prokaeva T, Lim A et al. Cardiac amyloidosis in African Americans: comparison of clinical and laboratory features of transthyretin V122I amyloidosis and immunoglobulin light chain amyloidosis. Am Heart J 2009; 158: 607–14. 6. Ng B, Connors LH, Davidoff R et al. Senile systemic amyloidosis presenting with heart failure: a comparison with light chain-associated amyloidosis. Arch Intern Med 2005;165: 1425–9. 7. Ruberg FL, Maurer MS, Judge DP et al. Prospective evaluation of the morbidity and mortality of wild-type and V122I mutant transthyretin amyloid cardiomyopathy: the Transthyretin Amyloidosis Cardiac Study (TRACS). Am Heart J 2012; 164: 222–8.e1. 8. Sekijima Y, Uchiyama S, Tojo K et al. High prevalence of wild-type transthyretin deposition in patients with idiopathic carpal tunnel syndrome: a common cause of carpal tunnel syndrome in the elderly. Hum Pathol 2011;42: 1785–91. 9. Ackermann EJ, Guo S, Booten S et al. Clinical development of an antisense therapy for the treatment of transthyretin-associated polyneuropathy. Amyloid 2012; 19 (Suppl. 1): 43–4. 10. Maurer MS, Grogan DR, Judge DP et al. Tafamidis in transthyretin amyloid cardiomyopathy: effects on transthyretin stabilization and clinical outcomes. Circ Heart Fail 2015; 8: 519–26. 11. Obici L, Cortese A, Lozza A et al. Doxycycline plus tauroursodeoxycholic acid for transthyretin amyloidosis: a phase II study. Amyloid 2012; 19 (Suppl. 1): 34–6. 12. Wu SY, Lopez-Berestein G, Calin GA et al. RNAi therapies: drugging the undruggable. Sci Transl Med 2014; 6: 240ps7. 13. Benson MD. Liver transplantation and transthyretin amyloidosis. Muscle Nerve 2013; 47: 157–62. 14. Carvalho A, Rocha A, Lobato L. Liver transplantation in transthyretin amyloidosis: issues and challenges. Liver Transpl 2015; 21: 282–92. 15. Ericzon BG, Wilczek HE, Larsson M et al. Liver Transplantation for hereditary transthyretin amyloidosis: after 20 years still the best therapeutic alternative? Transplantation 2015;99: 1847–54. 16. Maia LF, Magalhes R, Freitas J et al. CNS involvement in V30M transthyretin amyloidosis: clinical, neuropathological and biochemical findings. J Neurol Neurosurg Psychiatry 2015;86: 159–67. 17. Oshima T, Kawahara S, Ueda M et al. Changes in pathological and biochemical findings of systemic tissue sites in familial amyloid polyneuropathy more than 10 years after liver transplantation. J Neurol Neurosurg Psychiatry 2014; 85: 740–6. Источник: http://con-med.ru/ | |
| Просмотров: 1567 | |
| Всего комментариев: 0 | |